Differenzialdiagnosen bei negativem Entzündungsbefund
Bei Patient:innen mit rheuma-ähnlichen Beschwerden ohne auffällige Entzündungswerte im Blut kommt der ausführlichen Anamnese und der sorgfältigen körperlichen Untersuchung besondere Bedeutung zu. Es ist möglich, dass sich die rheumatische Erkrankung noch in einem frühen Stadium befindet und sich daher noch nicht im Blutbild widerspiegelt.ref_Suresh_2004
Ebenso ist es möglich, dass keine rheumatische Erkrankung vorliegt, sondern eine andere Ursache mit ähnlicher Symptomatik. Dazu zählen unter anderem Fibromyalgie, Borreliose, oder Arthrose.ref_Pfeil_2023ref_Online_2025 Auch Hypophosphatasie (HPP) ist eine mögliche Differenzialdiagnose, da sie Beschwerden verursachen kann, die leicht mit rheumatischen Erkrankungen verwechselt werden.ref_Feuerstein_2022
Hypophosphatasie vs. Rheuma: Symptome im Vergleich
HPP ist eine genetisch bedingte Systemerkrankung, deren klinische Manifestationen sich mit denen rheumatischer Erkrankungen wie Fibromyalgie und rheumatoide Arthritis überlappen können.ref_Feuerstein_2022 Die möglichen Manifestationen der HPP sind heterogen und reichen von muskuloskelettalen, gastrointestinalen und renalen Symptomen über dentale bis hin zu neurologischen Symptomen.ref_Schidt_2021ref_Seefried_2020 In manchen Fällen kann HPP mit einer erheblichen Einschränkung der Mobilität einhergehen, sodass Patient:innen auf Gehhilfen oder einen Rollstuhl angewiesen sein können.ref_Dahir_2023 Häufige Fehldiagnosen dieser Patienten sind zum Beispiel rheumatoide Arthritis oder Morbus Bechterew.ref_Rockman_2013ref_Beck_2009ref_Karakostas_2022
|
Häufige Symptome bei Hypophosphatasie-Patient:innen, die in der rheumatologischen Praxis vorstellig werden:ref_Bianchi_2020ref_Barvencik_2017 |
|
|---|---|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
Unterscheidungskriterium: Alkalische Phosphatase
Ein zentrales Merkmal der HPP ist eine zu niedrige Aktivität der alkalischen Phosphatase (AP) aufgrund einer Mutation des ALPL-Gens.ref_Whyte_2016 Dieses Enzym ist an der Dephosphorylierung einer Vielzahl von Substraten beteiligt, einschließlich anorganischem Pyrophosphat (PPi), Phosphatidylethanolamin (PEA) und Pyridoxal-5′-phosphat (PLP). Niedrige Konzentrationen der AP im Serum in Verbindung mit der Anreicherung dieser Substrate sind typisch für HPP. Der Anstieg des PPi-Spiegels kann zu Ablagerungen von Kalziumpyrophosphatdihydrat-Kristallen im Gelenkknorpel führen, was zur Chondrokalzinose und Enthesiopathie führt und bei HPP-Patient:innen Schmerzen des Bewegungsapparates verursachen kann.ref_Alonso_2009
Da diese Parameter im Standard-Rheumalabor häufig nicht enthalten sind, sollten Rheumatolog:innen bei atypischen oder therapieresistenten Verläufen gezielt den AP-Wert überprüfen.
Studiendaten zu HPP im Rheuma-Patientenkollektiv
Im Rahmen einer retrospektiven Studie am Universitätsklinikum Bonn wurden die Daten von 2.289 erwachsenen Patient:innen mit rheumatischen Symptomen untersucht.ref_Barvencik_2017 Ziel war es, herauszufinden, ob bei diesen Patient:innen pathologisch erniedrigte Werte der alkalischen Phosphatase (AP < 35 U/l) vorlagen. Insgesamt wiesen 30 Patient:innen eine persistierend niedrige AP-Aktivität auf. Bei 28 bestand Verdacht auf HPP, bei 19 dieser Patient:innen konnten genetische Untersuchungen erfolgen. Davon wiesen wiederum 13 Patient:innen eine pathogene Variante des ALPL-Gens auf.
Somit ergab sich innerhalb des gesamten analysierten Patientenkollektivs mit rheumatologischen Erkrankungen eine Prävalenz von 0,57 % – also etwa 1 von 200 Patient:innen. Im Kollektiv der Patient:innen mit persistierend niedriger AP-Aktivität lag die Prävalenz bei 43,3 %.ref_Barvencik_2017 Eine weitere Studie aus Spanien zeigte vergleichbare Ergebnisse.ref_Garcia_2019
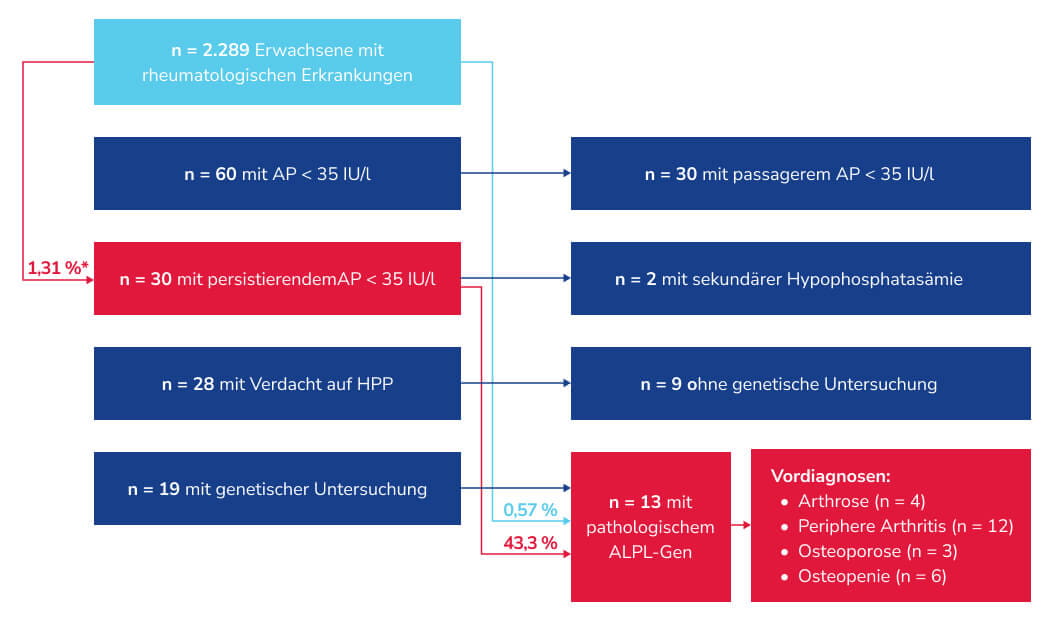

Abb. adaptiert nach Karakostas P et al., 2022.




Mehr Infos zum Thema
Referenzen
- Pfeil A et al., Rheumatologie kompakt. Elsevier Health Sciences. 2023; 1. Auflage.
- Zeidler H et al., Differenzialdiagnose rheumatischer Erkrankungen. Springer-Verlag. 2018; 5. Auflage.
- Jansen N et al., Rheumatology Advances in Practice. 2023; 7(3),rkad076.
- De Stefano L et al., Clin Exp Rheumatol. 2023; 41(3):554-564.
- Suresh J et al., R Soc Med 2004; 97:421–424.
- Online unter: https://www.uptodate.com/contents/diagnosis-and-differential-diagnosis-of-rheumatoid-arthritis (Letzter Aufruf: 10.04.2025).
- Feurstein et al., Orphanet Journal of Rare Diseases. 2022; 17:435.
- Schmidt et al., Orphanet J Rare Dis. 2021; 16:45.
- Seefried L et al., JBMR. 2020; 35(11):2171–2178.
- Dahir KM et al., Front Endocrinol. 2023; 14:1138599.
- Rockman-Greenberg C, Pediatr Endocrinol Rev. 2013; 10:380–388.
- Beck C et al., The Open Bone J. 2009; 1:8–15.
- Karakostas P et al., Z Rheumatol. 2022; 81(6):513–519.
- Bianchi ML et al., Osteoporos Int. 2020; 31(8):1445–1460.
- Barvencik F et al., Thieme-Refresher Rheumatologie. 2017; 10:13–24.
- Whyte MP, Nat Rev Endocrinol. 2016; 12(4):233–46.
- Alonso G et al., Med Clin 2009;132:108–111.
- García-Fontana C et al., Sci Rep. 2019; 9:9569.
Hinweis: Die hier bereitgestellten Informationen dienen der ärztlichen Fortbildung und ersetzen nicht die individuelle klinische Beurteilung im Einzelfall. Bei spezifischen Fragestellungen konsultieren Sie bitte die aktuellen Leitlinien der entsprechenden Fachgesellschaften.
.jpg?h=420&iar=0&w=1900&hash=4DDE6CC6229988E78C58AADC655144A9)




