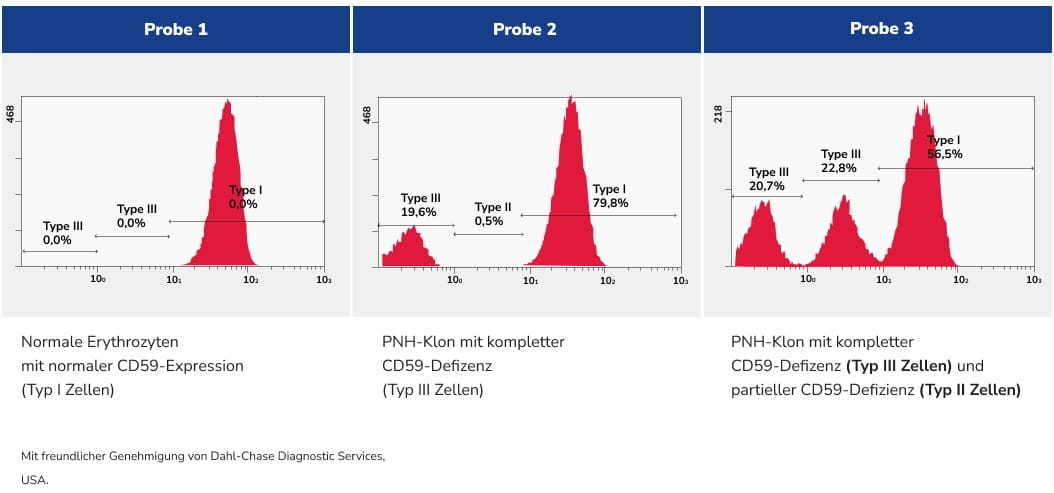
Zusammenfassung PNH-Diagnostik mittels Durchflusszytometrie:
Eine geeignete Untersuchung beinhaltet:
- Durchflusszytometrie von peripherem Blutref_Borowitz_2010ref_Schrezenmeier_2011
- Messung der Granulozyten und mindestens einer weiteren Zellreihe, z. B. Monozyten. Werte für Erythrozyten können abweichen aufgrund der Zerstörung durch die intravasale Hämolyse ref_Borowitz_2010ref_Schrezenmeier_2011
- Verwendung von mindestens zwei Antikörpern zur Detektion GPI-verankerter Proteine (z. B. CD59 und CD55) oder FLAER<ref_Borowitz_2010ref_Schrezenmeier_2011
- Sensitivität: 1 % bei Routinekontrollen und deutlich höhere Sensitivität bei Patient:innen mit aplastischer Anämieref_Borowitz_2010
- Klongröße für jede untersuchte Zellreiheref_Borowitz_2010

| Untersuch. |
Anmerkungen |
| Anamnese | |
| Allgemeine Familien-/ Eigenanamnese | Diskriminierung zwischen erworbener Störung und kongenitalen Differenzialdiagnosen (z.B. Membranopathien, Enzymopathien) |
| PNH-typische Symptome | Anämie-Symptomatik, Fatigue, Dyspnoe, Urinverfärbung, rekur- rente abdominelle Schmerzkrisen, Dysphagie, Kopfschmerzen, erektile Dysfunktion, TE-Ereignisse, Blutungszeichen |
| Komorbiditäten |
|
| Transfusionshistorie |
|
| Aktuelle Medikation | z.B. Kortikosteroide, Anabolika, Vit. D oder Folsäure-Supplemente |
| Impfhistorie | Im Hinblick auf eine geplante Komplementinhibitortherapie |
| Frage nach Lebensplanung bei Frauen |
|
| Körperliche Untersuchung | |
| Anämie-Zeichen, Ikterus, Hinweise für akute od. abgelaufene Thrombosen, Blutungszeichen, konstitutionelle Auffälligkeiten wie bei kongenitalen aplastischen Anämien, Splenomegalie | |